鈦及鈦合金屈服強度高、密度低,具有良好的力學性能,優異的耐蝕性和抗沖刷性,[1?2],廣泛運用于海洋工程領域,特別是海水管路和海水冷卻發電裝置等[3?5]。雖然鈦合金具有良好的耐蝕性,但在惡劣的海洋環境中同樣面臨著海水腐蝕問題。海水腐蝕是由多種因素造成的,包括:鹽度、溫度、pH以及生物污損等,其中生物污損是最重要的因素之一[6]。
生物污損是一個復雜的過程,涉及微生物(包括細菌、原生動物和微藻)和大型污損生物(包括藤壺、牡蠣等大型無脊椎動物和大型藻類)[7?8]。微生物在材料表面附著會誘發腐蝕(MIC),這已經被廣泛研究[9?13]。如鈦合金在流動海水中形成的生物薄膜約20~50μm,短期內對材料具有保護作用[14]。Shewanella藻類通過削弱鈦合金鈍化膜,使Cl?更具侵略性,加劇腐蝕[15]。嗜鹽菌N.tibetense在Q235鋼表面非均勻局部聚集,形成氧濃差腐蝕電池誘發局部腐蝕,且N.tibetense能以Fe為能源物質獲取電子,加速電化學反應的電荷轉移,進而加速腐蝕進程,氧濃度差腐蝕電池和N.tibetense對鐵金屬直接消耗兩種機制耦合共同促進碳鋼腐蝕[16]。細菌產生的胞外聚合物質(EPS)可以使B30銅鎳合金表面形成較厚雙氧化層(外層沉積Cu2O層和內部氧化鎳層),有效減緩試樣腐蝕速率[17]。微生物附著對金屬的腐蝕影響已經得到很好的研究,不同微生物的生命活動對不同金屬材料的腐蝕行為亦有所差異[18?21]。馬士德等[22]在三亞對工業純鈦(TA2)進行海水腐蝕研究,結果表明致密、穩定的鈦氧化物膜起到了防腐作用,但污損生物群落演替導致防腐作用難以保證長期性和穩定性,尤其是局部環境。同時,已有研究表明,大型污損生物短期內對不銹鋼具有保護作用,但大型污損生物一般是長期且不均勻附著,易在污損生物與金屬材料的邊緣縫隙間形成氧濃度差,從而導致局部腐蝕[23?25]。在以往大型污損生物研究中,研究材料一般為不銹鋼和碳鋼,缺乏對鈦合金的研究和分析[26?27]。不同材料受海水理化性質和污損生物群落演替影響,腐蝕行為存在差異,且海水中材料腐蝕和污損生物的生命活動高度依賴特定的地理位置[28]。實驗室中通過培養污損生物進行研究往往不能還原特定海域的海水理化性質和生物多樣性。因此有必要在亞熱帶湛江灣實海研究污損生物附著行為對鈦合金的腐蝕影響。
本研究選取TC4鈦合金在湛江調順島實海中掛樣,觀察污損生物附著行為以及試樣腐蝕形貌,結合電化學測試和XRD研究污損生物附著對TC4鈦合金的腐蝕影響,探索生物腐蝕機理,為鈦合金在海洋工程裝備應用提供一定的理論和參考。
1、實驗材料和方法
1.1實驗材料
TC4鈦合金化學成分如表1所示。
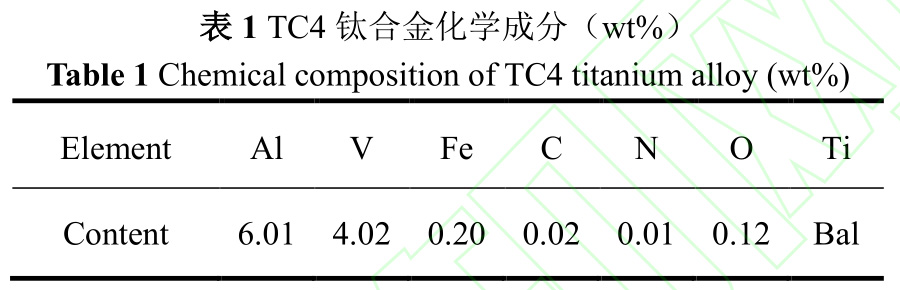
1.2實驗方法
1.2.1樣品制備
試樣加工尺寸為Φ56mmφ3mm,用240#、400#、800#、1000#砂紙將試樣表面打磨平整,將試樣浸泡在丙酮中,放入超聲波清洗儀清洗15分鐘后,使用無水乙醇和蒸餾水對試樣進行洗滌,干燥封裝、編號后放入干燥箱備用。試樣密封裝置采用帶螺紋管節,內部裝有金屬試樣,使用彈簧將導線壓在金屬試樣表面,管節一端使用環氧樹脂密封,另一端采用密封圈密封。由于密封作用,試樣實際上只有一面暴露于海水中。
1.2.2實驗內容與方法
樣品封裝后,于2022年9月6日投放在廣東湛江調順島海域,浸入海水中深度為2m,該海域全年月平均水溫16.3℃32.6℃,鹽度24.2‰26.9‰,pH8.108.22,濁度8.60FTU~13.6FTU。該海域漲、落潮平均流速分別為0.2m/s和0.24m/s,漲潮流速小于落潮流速,其比值為0.84。其中,大潮漲、落潮段平均流速分別為0.27m/s和0.30m/s;小潮漲、落潮段平均流速分別為0.14m/s和0.18m/s。
本實驗分為8組,每組設置3個平行樣,取樣周期為5、10、20、30、45、60、75和90d,每個實驗周期都從海水中取回3個平行樣,首先進行電化學測試,電解池采用三電極體系,參比電極(RE)為飽和KCl甘汞電極(SCE),輔助電極(CE)為20mm×20mm×0.2mm鉑電極,試樣為工作電極(WE),有效面積24.62cm2,電解質為海水。在開路電位下對試樣進行EIS測試,頻率范圍為0.01~105Hz,信號幅值為5mV正弦波。極化曲線掃描速率為0.5mV/s,掃描區間±0.01V(相對開路電位),采用Zview軟件對EIS進行等效電路擬合和分析。接著使用Nikon數碼相機拍攝宏觀形貌,將螺紋管節拆開取出試樣,采用XRD對試樣各個浸泡階段腐蝕產物進行分析,掃描2?角度10°~90°,掃描速率4(°)/min,步長0.04。
藤壺等大型污損生物使用鑷子去除鈣質外殼后,蒸餾水反復沖洗,然后按照GB/T16545-2015《金屬和合金的腐蝕腐蝕試樣上腐蝕產物的清除》配置除銹液去除藤壺基板和清洗試樣表面,接著用無水乙醇洗滌,最后用蒸餾水洗滌,干燥,最后使用徠卡超景深顯微鏡觀察表面微觀形貌。
2、結果與分析
22.1樣品形貌觀察與分析
圖1是TC4鈦合金在海水中浸泡不同時間的宏觀形貌。5d,試樣表面依然光亮,有幼體藤壺附著。10d,藤壺基底直徑增大,“生物泥”肉眼可見。20d,藤壺數量與個體呈上升趨勢,個別藤壺基底直徑達7mm,試樣約50%面積被覆蓋,“生物泥”厚度明顯增大,水螅、管棲多毛類泥管和石灰質管等開始附著,這些均為我國南海污損生物季節性優勢物種[29],也是“生物泥”主要構成,如圖2所示。“生物泥”的形成是細菌和硅藻等微生物膜加上有機或無機顆粒的運動、黏附和沉積作用,使微生物膜增厚形成“生物泥”[22]。30~45d,未觀察到其他新物種附著,藤壺基底直徑增大、數量增加,覆蓋面積達90%以上,表明鈦合金具有較好的生物相容性,是海洋生物的理想棲息地[30]。同時,部分藤壺死亡形成空殼,藤壺空殼在海水沖刷下脫落,但藤壺基底并未脫離試樣,表明藤壺膠具有較強粘性[31?32]。


60~75d,此時藤壺依然是試樣表面污損生物的優勢物種,此時污損生物覆蓋面積比高達99%。溫差過大可造成藤壺大面積死亡[33?36],而本實驗是在秋冬季進行,75~90d時湛江海域進入冬季,受季節影響溫度驟變,導致藤壺大部分死亡,死亡率達95%。
圖3是TC4鈦合金在海水中浸泡不同時間藤壺附著數量及面積占比。從圖中可以看出10d時藤壺附著數量最少,為1.3pcs/cm2,結合圖1可知在試驗初期,試樣表面較為光滑,幼體藤壺附著強度較小[33],部分幼體藤壺在海水沖刷下脫落或死亡脫落。20d時,試樣表面藤壺數量明顯增多,個體基底直徑明顯增大。隨著試驗時間延長,試樣表面粗糙度和“生物泥”厚度逐漸增大,且部分藤壺生長成熟,開始繁殖[37],使得試樣表面藤壺附著數量在30d時最多,為4.5pcs/cm2。之后藤壺基底直徑不斷增大,附著空間被壓縮,幼體藤壺擠壓脫落以及部分藤壺死亡脫落,藤壺附著數量波動變化,但整體覆蓋面積占比幾乎不變。
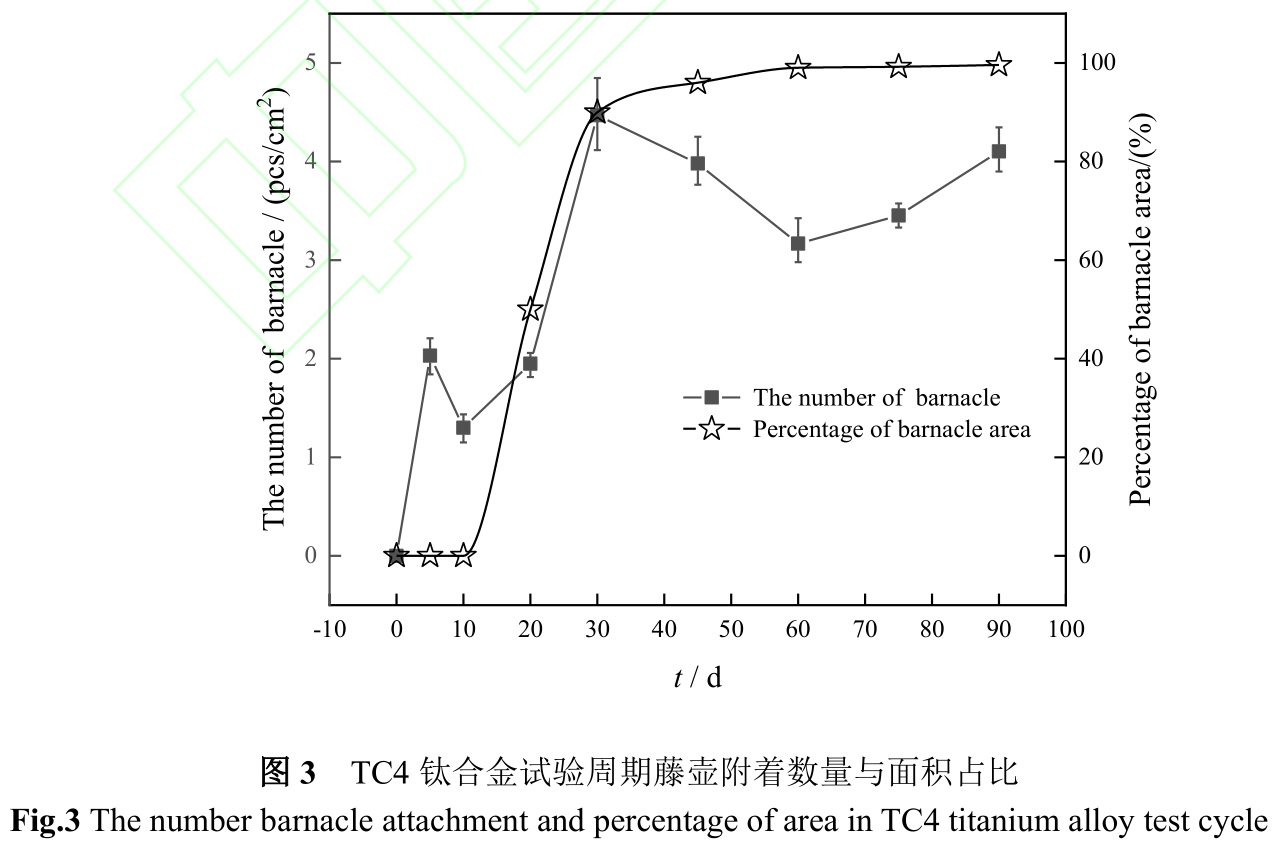
圖4是TC4鈦合金去除表面附著物后的微觀形貌圖。結合圖1和圖4可知,在海水中浸泡的前10d,鈦合金表面主要是由微生物組成的生物膜,同時也是鈦合金鈍化膜形成階段,微生物膜的形成造成介質不均勻性導致鈦合金鈍化膜不均勻,表面呈現密集的小而淺的缺陷;在海水中浸泡30d后,鈦合金表面主要污損生物演替為藤壺,隨藤壺生長與死亡,在生長過程中藤壺體現較好的阻隔作用,鈦合金鈍化膜基本完整,表面呈現小而淺的缺陷;藤壺死亡后,藤壺阻隔性下降,藤壺內部有機質分解造成低氧海水環境,從而使鈦合金鈍化膜再生困難,并且藤壺下鈦合金與藤壺外鈦合金之間形成強烈的氧濃差,構成氧濃差電池,藤壺下鈦合金發生較快腐蝕,呈現大而深的腐蝕坑。

圖5是試樣表面3D微觀圖。試驗中后期(45~90d),試樣表面無藤壺附著位置或藤壺與藤壺空隙之間無明顯蝕坑,而藤壺附著位置出現蝕坑。隨著時間延長,藤壺附著位置點蝕更加密集或形成潰瘍坑,60d時潰瘍坑直徑高達1.5mm,90d時蝕坑最深可達0.14mm。

藤壺引起腐蝕需要具備三個條件:附著藤壺死亡、微生物對死亡藤壺有機體作用和構成宏觀電池[38]。海洋污損生物附著以及生命活動新陳代謝產生大量代謝產物和酸性物質,富集在試樣表面形成生物膜,從而在金屬和生物膜之間形成局部厭氧區,進而破壞鈍化膜,為海水中腐蝕性離子提供通道,促進腐蝕[39]。由圖1和圖5可知,藤壺在30d開始出現死亡,鈣質外殼被破壞和有機體被海水中微生物分解,為Cl?與材料表面的接觸、傳輸提供路徑,從而導致鈍化膜破裂。同時藤壺殼內第一觸角位置易形成活化點成為陽極與殼外金屬作為陰極構成宏觀電池,促進局部腐蝕。不同生長階段的藤壺對TC4鈦合金的腐蝕機制有所不同,結構完整的活體藤壺鈣質外殼和致密藤壺膠能夠有效隔離外界腐蝕介質,死亡藤壺則因殼體結構不完整與有機體被微生物分解,反而促進腐蝕。
2.2電化學測試結果與分析
(1)極化曲線
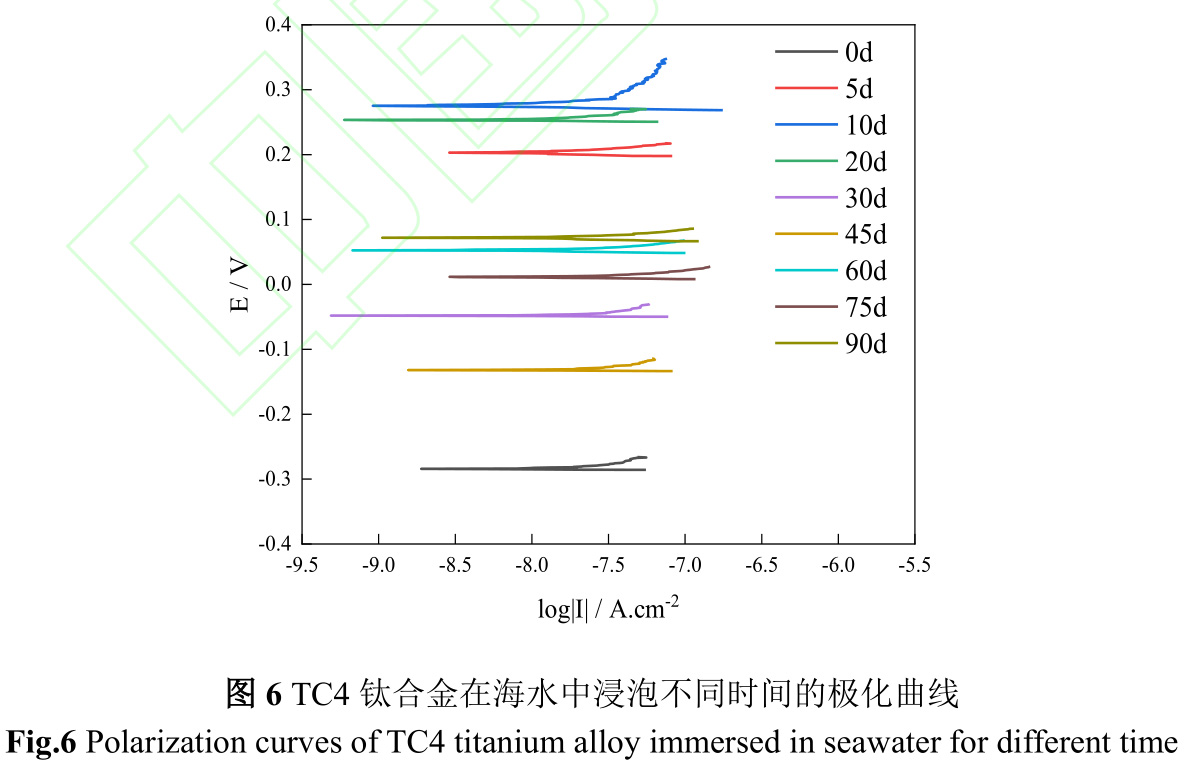
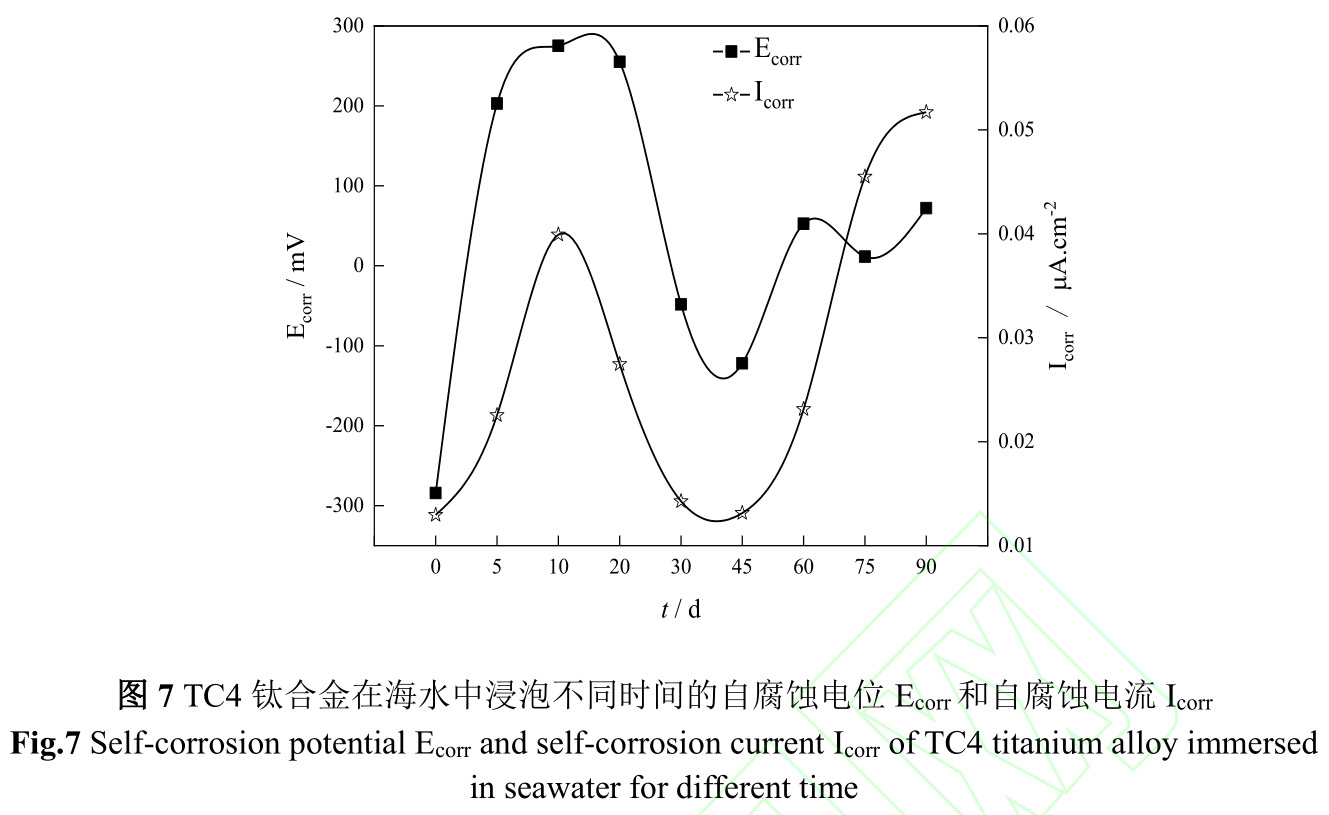
圖6是TC4鈦合金在海水中浸泡不同時間極化曲線,圖7是TC4鈦合金在海水中浸泡不同時間的自腐蝕電位(Ecorr)和自腐蝕電流(Icorr)。由圖6、7可知,TC4鈦合金在海水中初始腐蝕電位較負,為?284.2mV,隨著試驗時間延續,腐蝕電位急劇正移,腐蝕電流伴隨腐蝕電位而升高,在第10d,腐蝕電流達到最大,該階段金屬表面陽極溶解過程加速,從而增加了鈦合金腐蝕速度。第10d至45d,鈦合金腐蝕電位逐漸下降,腐蝕電流亦逐漸下降,結合圖1污損生物由微生物、小型生物組成生物淤泥層向以藤壺為主要的大型污損生物層轉變,金屬表面陽極溶解過程受到抑制,從而減緩鈦合金腐蝕速度。第45d后,以藤壺為主的大型污損生物大面積死亡,改變了鈦合金表面腐蝕環境,導致腐蝕電位升高的同時腐蝕電流也升高。
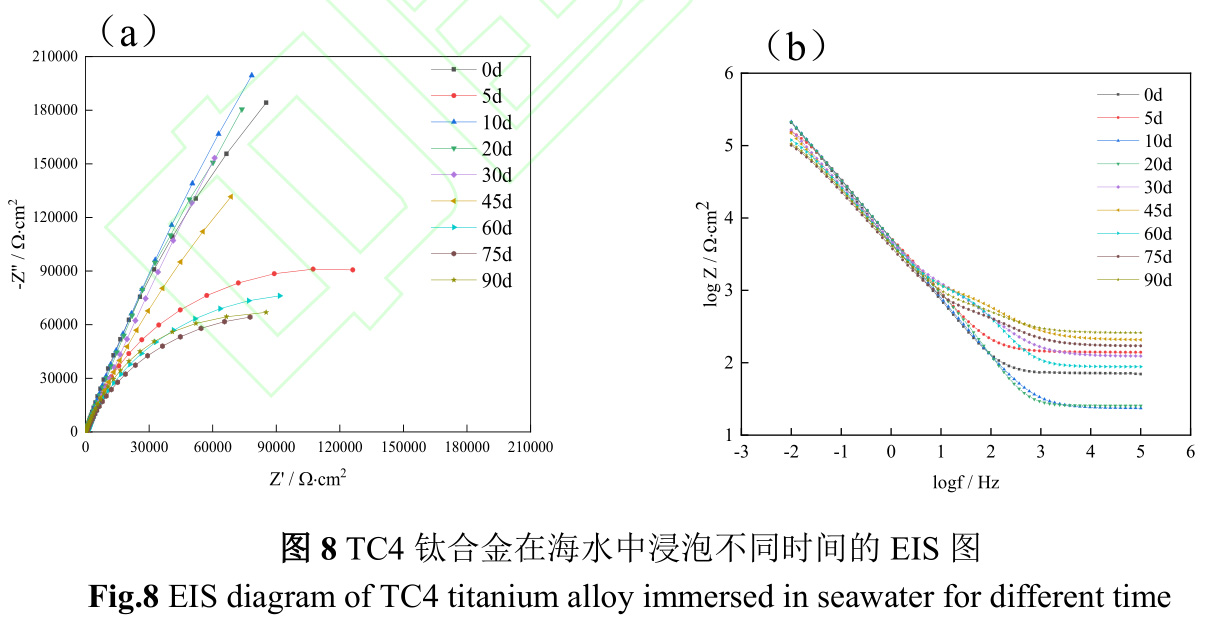
(2)EIS
圖8為TC4鈦合金在海水中浸泡不同時間的EIS圖。由圖1、2、7和圖8中的Nyquist圖可知,TC4鈦合金在浸泡初期(0~10d),生物膜附著與金屬表面鈍化膜致密化同時發生,容抗弧半徑先減小再增大,第10d時達到最大,此時材料耐蝕性較好。試驗中期(20~45d),容抗弧半徑逐漸減小,但幅度相對較小,生物膜的形成-脫落以及藤壺為主大型污損生物的附著-生長,影響了鈍化膜再生。試驗后期(60~90d),容抗弧半徑波動變化但明顯小于試驗前中期(0~45d),表明試驗后期材料耐蝕性較差,腐蝕趨勢較大。
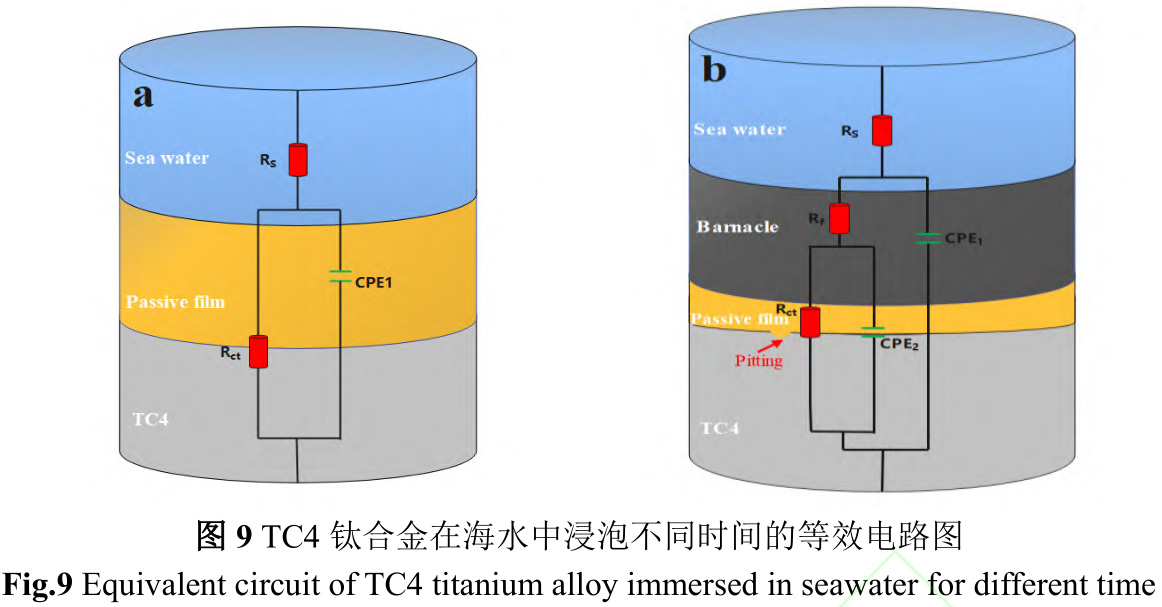
為定量分析TC4鈦合金與溶液界面之間的變化關系,采用圖9的等效電路圖對EIS進行擬合。試樣浸泡前,表面沒有生物膜和污損生物附著,采用單層膜模型Rs(CPE1Rct),試樣浸泡到海中,生物膜和污損生物的影響采用雙層膜模型Rs(CPE1(Rf(CPE2Rct)))。其中,Rs是溶液電阻,CPE1是膜電容,Rf是膜電阻,Rct是電荷轉移電阻,CPE2是溶液雙電層電容。以Rs(CPE1Rct)和Rs(CPE1(Rf(CPE2Rct)))兩種物理模型擬合的等效電路參數如表2所示。
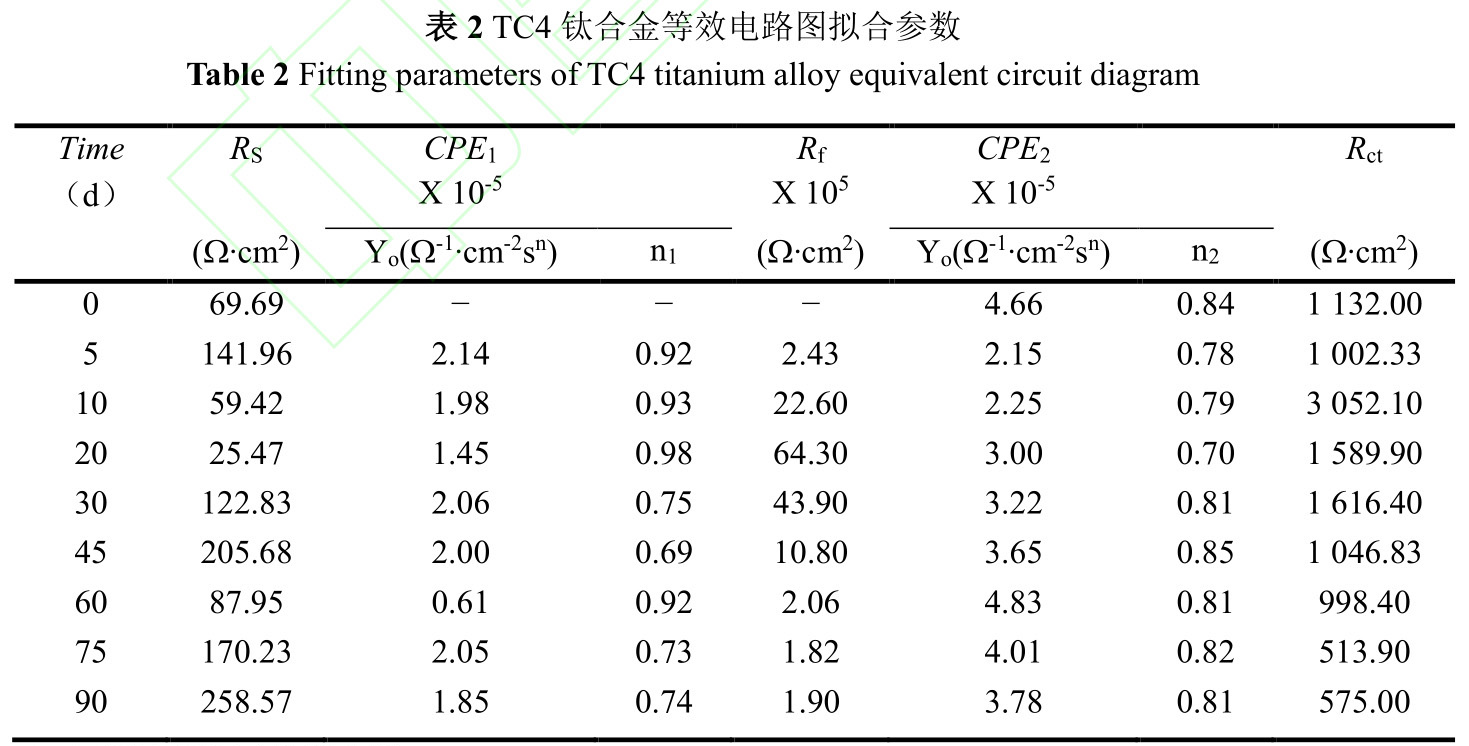
電化學測試溶液取自海中,不同試驗周期海水濁度、鹽度等理化參數受氣候影響并不一致,導致溶液體系相對不穩定,其中溶液電阻Rs最大值為258.57Ω.cm2,最小值為25.47Ω.cm2,最大偏差為233.1Ω.cm2。Rp為極化電阻,等于電荷轉移電阻Rct與膜電阻Rf的代數和,用于衡量材料抵抗腐蝕介質穿透能力的大小,與金屬腐蝕速度呈負相關。從擬合結果來看,在試驗初期(0~10d),第5d的Rp明顯小于第10d,表明浸泡初期鈍化膜致密性較差,該階段污損生物膜附著與鈦合金表面鈍化膜增厚、致密化過程。第10d至45d的Rp依舊處于較高水平,結合圖1可知第10d后污損生物由微生物、小型生物組成生物淤泥層向以藤壺為主要污損生物的大型污損生物層轉變,大型污損生物層相對生物淤泥層輸氧效率高,鈍化膜再生能力較強,阻滯了陽極溶解,腐蝕速度有所降低。試驗后期(60~90d),藤壺大量死亡,死亡藤壺造成鈦合金表面介質性質不均勻化[40],影響鈦合金表面鈍化膜形成與再生,使Rp降低,從而導致腐蝕速度增大。整個試驗中,污損生物附著影響鈦合金表面鈍化膜的形成與再生,從而影響整個腐蝕進程。
2.3腐蝕產物及機理分析
圖10是TC4鈦合金在海水中浸泡不同時間的XRD圖。TC4鈦合金為鈦鋁合金,在海水環境中,TC4鈦合金表面形成含有TiO2和Al2O3的鈍化膜,而CaCO3主要來源于鈣質外殼污損生物。CaCO3衍射峰從第10d出現,到第20d峰型尖銳,此演變規律與污損生物演替規律相同。在20~45d期間,CaCO3衍射峰呈增強-減弱-增強的波動變化,這是因為鈣質外殼污損生物局部附著,而XRD分析區域與鈣質外殼污損生物附著區域錯致所致。
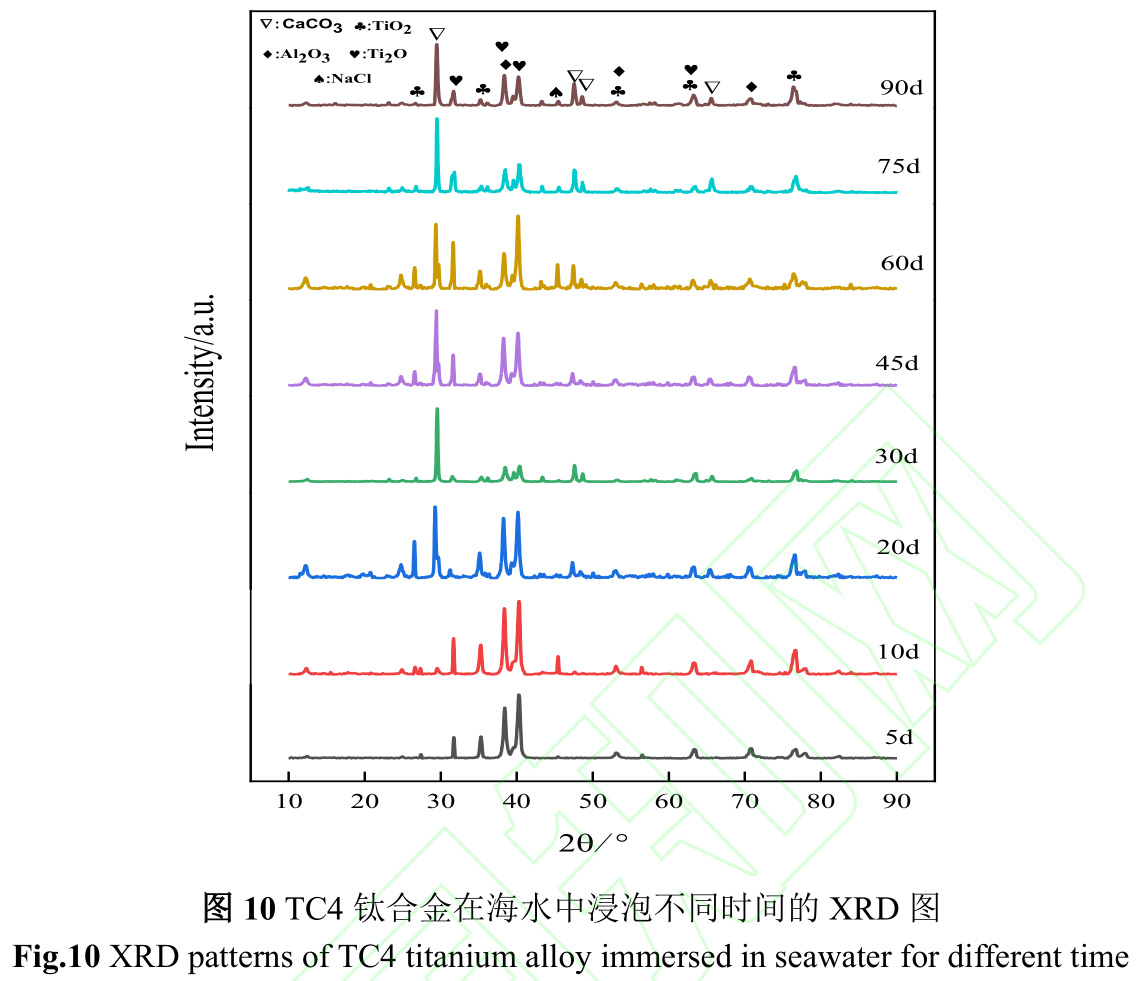
圖11是TC4鈦合金在海水中的腐蝕機理圖。鈦合金具有優良的耐蝕性是因為表面易形成鈍化膜,鈦合金在海水中鈍化反應如下:
Ti+2H2O→TiO2+4H++4e?(1)
2TiO2+2H++2e?→Ti2O3+H2O(2)
Ti2O3穩定性較差,會再次被氧化成TiO2:
Ti2O3+H2O→2TiO2+2H++2e?(3)
鈦合金鈍化和污損生物附著幾乎同時發生。Venkatesan等[41]研究表明海洋污損生物附著是長期且復雜的自然選擇、生態演替過程。通常材料浸沒在海水后,幾分鐘內被多聚糖和糖蛋白等有機分子與無機化合物快速黏附,形成基膜。浮游細菌利用范德華力等弱作用力在基膜上附著,通過新陳代謝產生具有黏性的細胞外高聚物[42],使附著逐漸牢固,最終形成生物膜。生物膜形成為藤壺幼蟲等大型污損生物附著提供了良好條件。生物膜形成和大型污損生物附著使試樣表面形成“生物封閉滯留層”,試樣不再直接與海水接觸。“生物封閉滯留層”是封閉或半封閉狀態,污損生物在試樣表面所占面積越大,對材料整體性保護越好[43]。
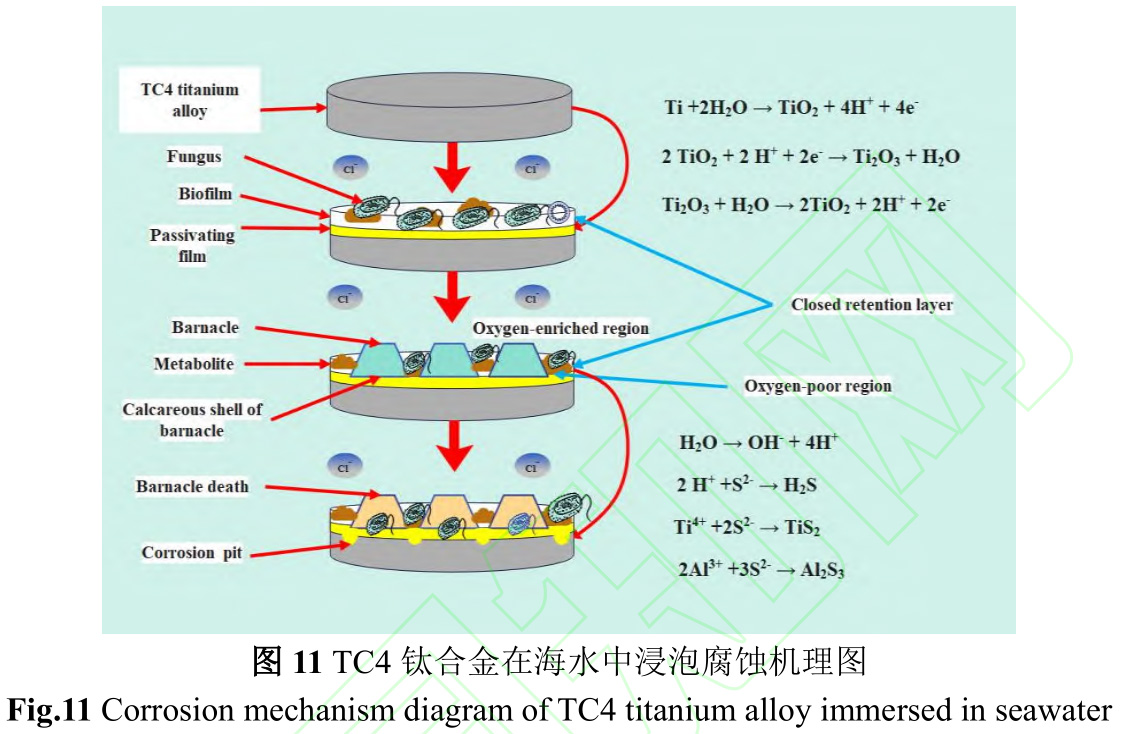
但由于大型污損生物不均勻附著以及存在耗氧和產氧生物,易造成不同區域氧濃度差異,形成氧濃差電池,富氧區作為陰極接受電子發生還原反應(反應4),貧氧區作為陽極失去電子發生氧化反應(反應5),由表1可知TC4鈦合金主要成分為Ti和Al,那么陽極發生是主要反應如反應6、7所示,形成局部腐蝕(反應8、9),表現為如圖5所示的潰瘍坑或較為密集點蝕。
O2+2H2O+4e?→4OH?(4)
M→M+++2e?(5)
Ti?2e?→Ti2+(6)
Al?3e?→Al3+(7)
Al3++3Cl?→AlCl3(8)
4AlCl3+3O2→2Al2O3+6Cl2(9)
Sangeetha等[44]認為藤壺膠能夠破壞鈍化膜,為海水中的Cl?等鹵素腐蝕性離子提供了通道,從而導致腐蝕不斷發展。而Eashwar等[45]認為藤壺死亡是材料發生局部腐蝕的先決條件。圖1中第30d開始發現有藤壺死亡,結合圖5的3D微觀圖局部腐蝕情況可知與Eashwar等的研究更相符。藤壺死亡后,藤壺有機體被好氧細菌分解產生酸性物質,降低藤壺殼內溶液pH,而酸性物質沿著藤壺殼基底中心向試樣表面滲透,最后發生局部腐蝕。
3、結論
1.鈦合金在海水中的腐蝕規律受污損生物演替規律影響。不同生長階段的藤壺對TC4鈦合金的腐蝕機制有所不同,結構完整的活體藤壺鈣質外殼和致密藤壺膠能夠有效隔離外界
腐蝕介質,死亡藤壺則因殼體結構不完整與有機體分解,促進腐蝕發生。
2.污損生物附著改變海水中的溶解氧向鈦合金表面傳輸效率,從而影響鈍化膜的形成與再生,同時造成鈦合金表面介質性質不均勻化,促成局部腐蝕發生。
3.藤壺等污損生物不均勻附著形成“封閉滯留層”,導致出現富氧區和貧氧區,構成氧濃差電池。富氧區作為陰極接受電子發生還原反應,貧氧區作為陽極失去電子發生氧化反應,促進局部腐蝕。TC4鈦合金在海水、鈍化膜和污損生物附著協同作用下,腐蝕速度非線性波動變化。
參考文獻
[1] 王海杰, 王佳, 彭欣等. 鈦合金在 3.5%NaCl 溶液中的腐蝕行為[J].中國腐蝕與防護學報,2015, 35(1): 75-80.
WANG H J, WANG J, PENG X, et al. Corrosion Behavior of Three Titanium Alloys in 3.5%NaCl Solution[J]. Journal of Chinese Society for Corrosion and Protection, 2015, 35(1):75-80.
[2] 訾群.鈦合金研究新進展及應用現狀[J].鈦工業進展, 2008, 25(2): 23-27.
ZI Q. New Development of Titanium Alloy and Its Application Actuality[J]. Titanium Industry Progress, 2008, 25(2): 23-27.
[3] GORYNIN I V. Titanium Alloys for Marine Application[J]. Materials Science and Engineering, 1999, 263(2), 112-116.
[4] WAKE H, TAKAHASHI H, TAKIMOTO T, et al. Development of An Electrochemical Antifouling System for Seawater Cooling Pipelines of Power Plants Using Titanium[J].Biotechnology and Bioengineering, 2006, 95(3), 468-473.
[5] 王廣夫.艦船海水管路系統防腐防污技術進展[J].材料開發與應用, 2016, 31(4): 108-112.
WANG G F. Development of Anti-corrosion and Fouling of Seawater Pipe System of Marine Ship[J]. Development and Application of Materials, 2016, 31(4): 108-112.
[6] LAQUE F L. Topics for Research in Marine Corrosion[J]. Materials Performance, 1982, 21,13-18.
[7] MARTIN W. Marine Epibiosis 1. Fouling and Antifouling - Some Basic Aspects[J]. Marine Ecology Progress Series, 1989, 58: 175-189.
[8] VINAGRE P A, SIMAS T, CRUZ E, et al. Marine Biofouling: A European Database for the Marine Renewable Energy Sector[J]. Journal of Marine Science and Engineering, 2020, 8(7):495-522.
[9] XU D K, ZHOU E Z, ZHAO Y, et al. Enhanced Resistance of 2205 Cu-bearing Duplex Stainless Steel Towards Microbiologically Influenced Corrosion by Marine Aerobic Pseudomonas Aeruginosa Biofilms[J]. Journal of Materials Science & Technology, 2018, 34,1325-1336.
[10] MACHUCA L L, BAILEY S I, GUBNER R, et al. Effect of Oxygen and Biofilms on Crevice Corrosion of UNS S31803 and UNS N08825 in Natural Seawater[J]. Corrosion Science,2013, 67, 242-255.
[11] MACHUCA L L, JEFFREY R, BAILEY S I, et al. Filtration-UV Irradiation as an Option for Mitigating the Risk of Microbiologically Influenced Corrosion of Subsea Construction Alloys in Seawater[J]. Corrosion Science, 2014, 79, 89-99.
[12] XU D K, LI Y C, GU T Y. Mechanistic Modeling of Bio-corrosion Caused by Biofilms of Sulfate Reducing Bacteria and Acid Producing Bacteria[J]. Bioelectrochemistry, 2016, 110,52-58.
[13] LI H B, ZHOU E Z, REN Y B, et al. Investigation of Microbiologically Influenced Corrosion of High Nitrogen Nickel-free Stainless Steel by Pseudomonas Aeruginosa[J].Corrosion Science, 2016, 111, 811-821.
[14] AL-MUHANNA K, HABIB K. Marine Biofouling of Different Alloys Exposed to Continuous Flowing Fresh Seawater by Electrochemical Impedance Spectroscopy[J]. Journal of Saudi Chemical Society, 2016, 20(4): 391-396.
[15] LI Z, WANG J, DONG Y Z, et al. Synergistic Effect of Chloride Ion and Shewanella Algae Accelerates the Corrosion of Ti-6Al-4V Alloy[J]. Journal of Materials Science & Technology,2021, 71, 177-185.
[16] 錢鴻昌.高鹽環境典型鋼鐵材料嗜鹽古菌微生物腐蝕行為機理研究[D].北京:北京科技大學, 2019.
QIAN H C. Study on Microbiologically Influenced Corrosion Behavior and Mechanism of Typical Steel and Iron Materials by Halophilic Archaea in High Salinity Environment[D].Beijing: University of Science and Technology Beijing, 2019.
[17] BAUTISTA B E T, WIKIEL A J, DATENKO I, et al. Influence of Extracellular Polymeric Substances (EPS) from Pseudomonas NCIMB 2021 on the Corrosion Behavior of 70Cu-30NiAlloy in Seawater[J]. Journal of Electroanalytical Chemistry, 2015, 737, 184-197.
[18] DUAN J Z, WU S R, ZHANG X J, et al. Corrosion of Carbon Steel Influenced by Anaerobic Biofilm in Natural Seawater[J], Electrochimica Acta, 2008, 54, 22-28.
[19] HAMZAH E, HUSSAIN M Z, Ibrahim Z, et al. Influence of Pseudomonas Aeruginosa Bacteria on Corrosion Resistance of 304 Stainless Steel[J]. Corrosion Engineering Science Technology, 2013, 48, 116-120.
[20] LI S L, QU Q, LI L, et al. Bacillus Cereus S-EPS as a Dual Bio-functional Corrosion and Scale Inhibitor in Artificial Seawater[J]. Water Research, 2019, 166, 1-11.
[21] Liu T, GUO Z W, ZENG Z S, et al. Marine Bacteria Provide Lasting Anticorrosion Activity for Steel Via Biofilm-induced Mineralization[J]. ACS Applied Materials Interfaces, 2018, 10,40317-40327.
[22] 馬士德,郭為民,劉欣,等.工業純鈦(TA2)在南海三亞海洋環境試驗站海水全浸的生物污損與腐蝕[J]. 海洋科學, 2018, 42(10): 23-30.
MA S D, GUO W M, LIU X, et al. Biofouling and Corrosion Analyses of Industrial Pure Titanium (TA2) Immersed in Seawater at Sanya Marine Environmental Test Station in South China Sea[J]. Marine Sciences, 2018, 42(10): 23-30.
[23] BLACKWOOD D J, LIM C S, TEO S L M, et al. Macrofouling Induced Localized Corrosion of Stainless Steel in Singapore Seawater[J]. Corrosion Science, 2017, 129, 152-160.
[24] DE BRITO L V R, COUTINHO R, CAVALCANTI E H, et al. The Influence of Macrofouling on the Corrosion Behavior of API 5L X65 Carbon Steel[J]. Biofouling, 2007, 193-201.
[25] BLACKWOOD D J, LIM C S, TEO S L M. Influence of Fouling on the Efficiency of Sacrificial Anodes in Providing Cathodic Protection in Southeast Asian Tropical Seawater[J].Biofouling, 2010, 26, 779-785.
[26] NEVILLE A, HODGKIESS T. Localised Effects of Macrofouling Species on Electrochemical Corrosion of Corrosion Resistant Alloys [J]. British Corrosion Journal, 2013,35, 54-59.
[27] NEVILLE A, HODGKIESS T. Comparative Study of Stainless Steel and Related Alloy Corrosion in Natural Sea Water[J]. British Corrosion Journal, 1988, 33(2), 111-120.
[28] DEXTER S C. Biofouling and Biocorrosion[J]. Bulletin of Electrochemistry, 1996, 12, 1-7.
[29] 嚴濤,張慧,李韻秋,等.污損性管棲多毛類生態特點及研究展望[J]. 生態學報, 2014, 34(21):6049-6057.
YAN T, ZHANG H, LI Y Q, et al. An Overview of Fouling Sedentary Polychaetes[J]. Acta Ecologica Sinica, 2014, 34(21): 6049-6057.
[30] 李爭顯,王浩楠,趙文.鈦合金表面海生物污損及防護技術的研究現狀和發展趨勢[J].鈦工業進展, 2015, 32(6): 1-7.
LI Z X, WANG H N, ZHAO W. Current Research Situation and Development Trend of the Biofouling and Antifouling Technology on Titanium Alloy[J]. Titanium Industry Progress, 2015, 32(6): 1-7.
[31] RAMAN S, KUMAR R. Interfacial Morphology and Nanomechanics of Cement of the Barnacle, Amphibalanus Reticulatus on Metallic and Non-metallic Substrata[J]. Biofouling,2011, 27(6): 569-577.
[32] LI C, WANG G, CHEN K Y, et al. Mechanical Analysis of A Scraping Method to Remove Attached Barnacles[J]. Journal of Marine Science and Engineering, 2020, 8(3): 150-164.
[33] CRISP D J, BOURGET E. Growth in Barnacles[J]. Advance in Marine Biology, 1985, 22:199-244.
[34] 鐵鏑,劉貴昌,劉曉軍,等.環境溫度對東方小藤壺(Chthamalus challengeri)生命表征的影[J].海洋環境科學, 2010, 29(2): 191-195.
TIE D, LIU G C, LIU X J, et al. Influence of Environmental Temperature on Vital Status of Barnacle: Chthamalus Challengeri[J]. Marine Environmental Science, 2010, 29(2): 191-195.
[35] SOUTHWARD A J. On the Behavior of Barnacles III. Further Observations on the Influence of Temperature and Age on Cirral Activity [J]. Journal of the Marine Biological Association of the United Kingdom, 1957, 36(2): 323-334.
[36] 李友熾,王貴,吳敬權,等.海洋污損生物藤壺生長過程及附著強度研究[J].海洋科學, 2023,47(8): 60-67.
LI Y C, WANG G, WU J Q, et al. Study on the Growth Process and Attachment Strength of Marine Fouling Barnacles[J]. Marine Sciences, 2023, 47(8): 60-67.
[37] WENDT D E, KOWALKE G L, KIM J, et al. Factors that Influence Elastomeric Coating Performance: the Effect of Coating Thickness on Basal Plate Morphology, Growth and Critical Removal Stress of the Barnacle Balanus Amphitrite[J]. Biofouling, 2006, 22(1): 1-9.
[38] 馬士德,謝肖勃,黃修明,等.藤壺附著對海水中金屬腐蝕的影響[J].中國腐蝕與防護學報,1995, 15(1): 74-78.
MA S D, XIE X B, HUANG X M, et al. The Effect of Barnacle Adhesion on Metal Corrosion in Seawater[J]. Journal of Chinese Society for Corrosion and Protection, 1995, 15(1): 74-78.
[39] ZHENG X W, ZHUANG X, LEI Y H, et al. Corrosion Behavior of the Ti-6Al-4V Alloy in Sulfate-Reducing Bacteria Solution[J]. Coatings, 2019, 10(1), 24.
[40] DENG P C, SHANGGUAN J Y, HU J Z, et al. Effect of Barnacles on the Corrosion Behavior of 304 Stainless Steel[J]. Metals, 2023, 13, 1649-1658.
[41] VENKATESAN R, MURTHY P S. Macro-fouling Control in Power Plants[M]. Berlin, Heidelberg: Springer, 2008.
[42] LEWIS J A. Marine Biofouling and Its Prevention on Underwater Surfaces[J]. Materials Forum, 1998, 22: 41-61.
[43] 馬士德. 金屬/海水界面兩個主要過程的關系[J].海洋湖沼通報, 1979, 02: 85-89.
MA S D. The Relationship of Two Main Process on Metal/Sea Water[J]. Transactions of Oceanology and Limnology, 1979, 02: 85-89.
[44] SANGEETHA R, KUMAR R, DOBLE M, et al. Barnacle Cement: An Etchant for Stainless Steel 316L[J]. Colloids and Surfaces B: Biointerfaces, 2010, 79(2), 524-530.
[45] EASHWAR M, SUBRAMANIAN G, CHANDRASEKARAN P, et al. Mechanism for Barnacle-Induced Crevice Corrosion in Stainless Steel[J]. Corrosion, 1992, 48(7), 608-612.
相關鏈接